Один из растительных белков по своему молекулярному поведению похож на прионы животных и грибов.
Prions, the misfolded proteins that are known for causing degenerative illnesses in animals and humans, may have been spotted for the first time in plants.
Researchers led by Susan Lindquist, a biologist at the Whitehead Institute for Biomedical Research in Cambridge, Massachusetts, report that they have found a section of protein in thale cress (Arabidopsis) that behaves like a prion when it is inserted into yeast.
In plants, the protein is called Luminidependens (LD), and it is normally involved in responding to daylight and controlling flowering time. When a part of the LD gene is inserted into yeast, it produces a protein that does not fold up normally, and which spreads this misfolded state to proteins around it in a domino effect that causes aggregates or clumps. Later generations of yeast cells inherit the effect: their versions of the protein also misfold.
This does not mean that plants definitely have prion-like proteins, adds Lindquist — but she thinks that it is likely. “I’d be surprised if they weren’t there,” she says. To prove it, researchers would need to grind up a plant and see whether they could find a protein such as LD in several different folded states, as well as show that any potential prion caused a misfolding cascade when added to a test-tube of protein. Lindquist adds that because she’s not a plant scientist — her focus is on using yeast to investigate prions — she hasn’t tried these experiments. The study is reported on 25 April in theProceedings of the National Academy of Sciences1.
Plant puzzle
It is not clear why LD might behave as a prion in plants. Prions are notorious for inducing ill effects: in humans, their misfolding and clumping can cause variant Creutzfeldt–Jakob Disease (vCJD); in sheep and goats, the same effect can cause scrapie. But Lindquist has shown that prion proteins can provide evolutionary advantages for some living organisms — such as, in yeast, surviving harsh environmental conditions.

Sam Ogden
Susan Lindquist uses yeast to investigate the roles of prions, misfolded proteins.
So the same might be true in plants, she speculates. Lindquist says that a clue could come from work done by other researchers, which has suggested that — in fruit flies — the build-up of prion-like proteins might help to form or stabilize long-term memories, by creating long-lived protein clusters at synapses2.
Plants also need to keep track of their outside environment, which is a kind of memory-formation: for example, some plants won’t flower until they have experienced many weeks of cold temperature. In the paper, Lindquist’s team suggest that if LD does act as a prion in plants, one of its functional roles might possibly be to create a permanent trace of outside temperatures through the accumulation of protein clusters.
Other plant scientists whom Nature contacted consider this idea to be extremely speculative. But, “it would be really cool to find that prion-like behaviour is playing a role in some normal aspect of plant development”, says Richard Amasino, a plant biochemist at the University of Wisconsin–Madison.
Lindquist is looking for more possible prions: her study picked out LD using a computerized algorithm to identify lengths of proteins in the thale cress plant that are similar to known yeast prions. The ability to switch between ‘normal’ and ‘misfolded’ states of folding “seems to be a fundamental property that a lot of proteins have”, she says.
Прионные заболевания – такие, как коровье бешенство или болезнь Крейцфельда-Якоба – возникают не по вине вирусов или бактерий, а из-за присутствия в клетках особых белков, называемых прионами.
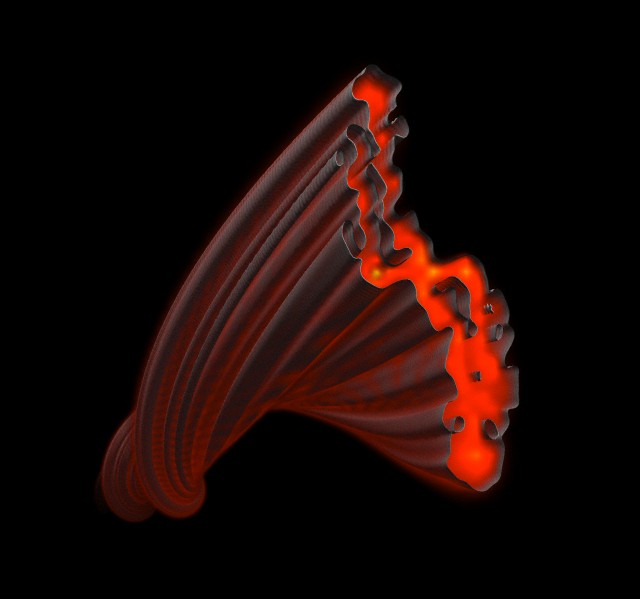
Структура белковой фибриллы, которая образуется в клетках при прионовых болезнях
Мы знаем, что любой белок – это уникальная последовательность аминокислот: у пищеварительного фермента пепсина она одна, у глобина в кровяных клетках – другая, у иммунного рецептора, сидящего на мембране лимфоцита – третья и т. д. Но белок не плавает по клетке в форме такой аминокислотной нитки, он сворачивается, приобретая уникальную и более-менее компактную пространственную конформацию. Сворачивание зависит от взаимодействий аминокислот между собой, и только в таком трёхмерном упакованном виде белок начинает работать, так как надо: расщеплять какие-то вещества, узнавать другие молекулы и пр.
В подавляющем большинстве случаев каждому виду белка присуща своя уникальная пространственная конформация. Но прионы могут сворачиваться разными способами, причём одна из форм становится инфекционной: если она столкнётся с молекулой, которая находится в нормальной конформации, то она переделает её под себя – нормальная молекула белка станет такой же, как инфекционная.
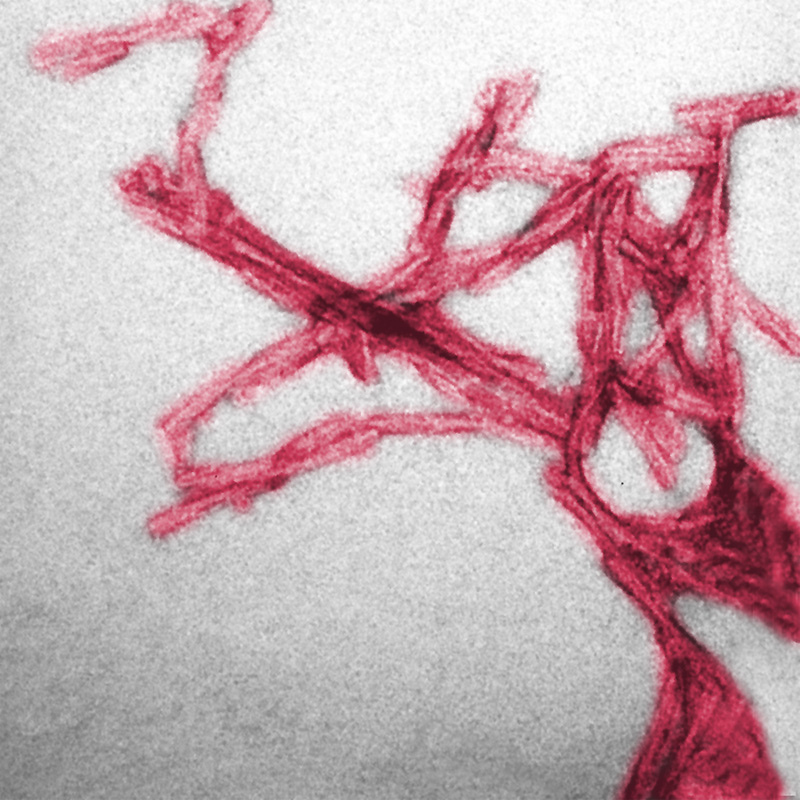
Прионовые фибриллы – нитевидные отложения, сформированные слипшимися друг с другом молекулами белка
Особенно неприятно то, что такая новая пространственная укладка заставляет прионы слипаться вместе, формируя отложения в виде характерных белковых нитей-фибрилл, которые вредят клетке и в конечном счёте убивают её. (Здесь необходимо отметить, что нормальная форма прионного белка клетке никак не вредит и выполняет в ней какие-то полезные функции.)
Похожим образом ведут себя белки, ответственные за болезнь Альцгеймера, болезнь Паркинсона – взаимодействуя друг с другом, они тоже образуют патогенные белковые комплексы, однако между ними и «истинными» прионами есть определённые отличия, о которых мы сейчас говорить не будем.
До сих пор считалось, что прионные белки есть только у животных и грибов, и проявляют они себя у них только в нервной системе. Потому столь необычными выглядят результаты группы Сьюзен Линдквист (Susan Lindquist) из Института биомедицинских исследований Уайтхеда – в своей статье в PNAS авторы пишут, что один из растительных белков ведёт себя как настоящий прион.
Исследователи прочесали около 500 белковых последовательностей резуховидки Таля, или арабидопсиса (Arabidopsis thaliana), ища среди них те, которые были бы похожи на прионы. В «улове» оказался белок Luminidependens (LD), правда, на прион был похож не весь LD, а только один его домен (так называют часть белка, которая структурно обособлена от остальной молекулы и часто обладает собственными функциями), впрочем, так же выглядят и дрожжевые прионы, у которых не вся молекула, а лишь часть её обладает «заразительными» свойствами.
Прионные свойства LD проверяли не в самом арабидопсисе, а в дрожжах. Его фрагмент, внедрённый в дрожжевые клетки, вёл себя, как настоящий прион: как только какая-то молекула приобретала инфекционную форму, так сразу же вокруг неё начинали формироваться белковые агрегаты, в которые вовлекались её соседи, перенявшие от неё «липучую» пространственную укладку.
Исследователи подчёркивают, что отсюда вовсе не следует, что и в растениях происходит то же самое – однако это весьма вероятно. И здесь стоит сказать, чем по-настоящему любопытны полученные результаты. В 2012 году Линдквист и её коллеги опубликовали в Nature статью, в которой говорили о полезной функции дрожжевых прионов: они помогали клеткам выживать в закисленной среде, в присутствии антигрибковых препаратов и при повышенном содержании этанола.
Один из прионных белков дрожжей в норме служит рибосомным «тормозом», прекращая синтез белка на определённом этапе, однако, когда молекулы «тормоза» начинают слипаться друг с другом, своей функции они выполнять уже не могут, и потому рибосома синтезирует удлинённые белки с каким-то новыми свойствам, которые, вероятно, помогают пережить стресс.
С другой стороны, эксперименты с дрозофилами показали, что у них такие белки помогают поддерживать долговременную память: белковые кластеры, образующиеся при слипании молекул прионов, служат укреплению межнейронных контактов – синапсов, а это значит, что нервные импульсы смогут беспрепятственно проходить по нейронной цепочке и информация, которая в ней хранится, не потеряется. (В данном случае прионы опять выступают в роли регуляторов белкового синтеза, подробнее про их роль в упрочении синаптических связей можно узнать из статей в Cell и PLoS ONE.)
Подобные исследования наводят на естественное предположение, что у всех прионов есть какие-то полезные функции – даже в том случае, когда они неправильно сворачиваются и слипаются. Возможно, прионное слипание и так происходит в клетках, просто здоровая клетка умеет держать процесс под контролем, а вот болезнь начинается, когда белковые комплексы формируются бесконтрольно и безостановочно.
Растительный белок LD может стать дополнительным аргументом в пользу такой теории: он участвует в регуляции суточного цикла растений и контролирует время цветения; по мнению авторов исследования, он благодаря своим прионным свойствам мог бы работать, к примеру, чем-то вроде предохранителя, не допуская появления цветков, пока ещё слишком холодно.
Однако подобные рассуждения всё-таки нужно обосновать экспериментально; пока же, напомним, прионные свойства самого LD получилось увидеть, только пересадив его в дрожжи. Но не исключено, что чем больше новых прионов мы обнаружим, тем больше будут меняться наши представления о них.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.







Сообщить об опечатке
Текст, который будет отправлен нашим редакторам: